【标题翻译】NAD+在急性脑损伤中调控线粒体自由基生成的作用
【文献作者】Nina Klimova, Adam Fearnow, Tibor Kristian
【发布杂志】Brain Sciences
【发布时间】2020.07
【影响因子】3.332
【文献解读】
线粒体是决定细胞存活和死亡的重要细胞器,任何线粒体功能紊乱都会对细胞存活产生不利影响。许多疾病都是因为线粒体功能障碍和线粒体异常引起的。因此,通过改善线粒体功能可以显著减轻疾病病理。线粒体自由基产生的增加被认为是疾病状态下对线粒体活性产生不利影响的主要原因。通常认为,过高水平的活性氧是导致急性脑损伤或神经退行性疾病中细胞死亡的重要因素。
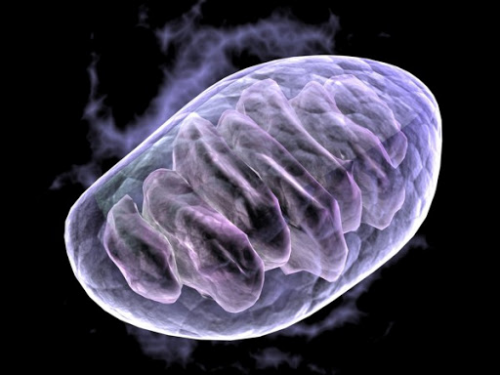
(注:图片摘自网络)
在生理条件下,线粒体产生的活性氧的量取决于活性氧的生成速率和清除速率。为了将活性氧维持在正常生理水平,大脑线粒体内存在一种清除活性氧的抗氧化防御系统,包括锰超氧化物歧化酶、谷胱甘肽、谷胱甘肽还原酶、谷胱甘肽过氧化物酶等。有趣的是,活性氧的产生和清除系统都依赖于NADH/NAD+的比例。因此,线粒体活性氧的产生清除都受到线粒体NAD+水平及其氧化还原状态变化的影响。
(注:图片摘自网络)
在心脏骤停引起的整体性脑缺血的情况下,脑组织中的氧气在几秒钟内就被耗尽了,这导致脑细胞,特别是神经元触发兴奋性毒性细胞死亡机制。通过恢复血流来恢复氧气是抢救脑组织的先决条件。但在早期缺血再灌注时会产生大量活性氧,诱导DNA损伤并激活DNA修复酶PARP1。该酶以NAD+作为底物,PARP1的过度活化会耗尽细胞内NAD+,进而耗尽细胞能量,导致大脑神经元死亡。研究表明,缺血性损伤后补充NAD+前体NMN可保护海马体神经元免受缺血性细胞死亡,保留神经元功能。
NAD+的作用还体现在蛋白去乙酰化酶SIRTs中。线粒体蛋白质乙酰化程度的提高对其活性具有抑制作用。缺血性损伤后NAD+水平显著降低,依赖于NAD+的SIRTs活性被抑制,因此线粒体蛋白在缺血损伤恢复的最初24小时内显示出过度的乙酰化,锰超氧化物歧化酶活性降低,活性氧清除功能受损。使用NAD+前体NMN治疗可阻止缺血后线粒体NAD+的减少,抑制了活性氧水平的增高。所有这些证据表明,通过使线粒体和细胞NAD+代谢正常化,可以逆转缺血后恢复期中活性氧的增加,避免大脑神经功能受损。
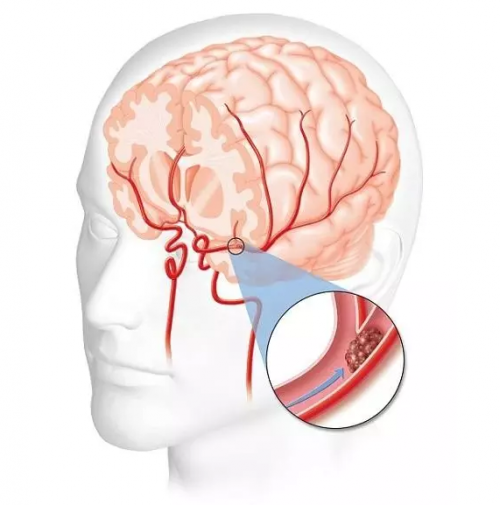
(注:图片摘自网络)
【文献总结】
线粒体是急性脑损伤后或神经退行性疾病发展过程中活性氧的主要来源。线粒体内NAD+耗竭引起的线粒体抗氧化系统受损是导致线粒体活性氧大量生成的主要机制。服用NMN可防止线粒体NAD+耗竭及其带来的负面影响。这或是一种改善大脑急性缺血损伤预后的新的治疗方法。
今天就分享这么多了,想要了解更多抗衰老最新的研究解读,可下载杉宝app。
杉宝APP主张以前沿的科学方式打造年轻态健康生活。其中主要包含抗衰老科学文献解读、shinebion抗衰老产品推荐、千万真实用户的分享体验等等,秉持科学的健康管理方式,帮助人们延缓衰老,尊享高品质生活。
【延伸阅读】
活性氧自由基:包括超氧阴离子自由基、羟自由基等,特点是含有一个不成对的电子,因此会夺取其他物质的电子,使自己稳定。体内活性氧自由基具有一定的功能,如免疫和信号传导过程。但过多的活性氧自由基就会有破坏行为,导致人体正常细胞和组织的损坏,从而引起多种疾病。
标签:
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。