快速分析CRISPR编辑的新工具揭示了意外编辑的频繁产生
特拉华州威尔明顿,2019年12月6日-在人们越来越希望使用CRISPR基因编辑工具修复与囊性纤维化和镰状细胞病等疾病相关的致命突变的过程中,《自然》杂志Communications Biology的一项新研究描述了一项可以加速创新的新创新通过快速揭示基因编辑过程中引入的意外变化和潜在有害变化来完成这项工作。
Eric Kmiec博士说:“我们已经开发出一种新方法,用于快速筛选CRISPR所做的所有编辑,结果表明,CRISPR修复位点周围的DNA可能有比原先想象的更多的意外变化,” Eric Kmiec博士说,克里斯蒂安娜·卡雷(ChristianaCare)基因编辑研究所所长和该研究的主要作者。
这项研究描述了由基因编辑研究所开发的一种新工具,该工具仅需48小时即可识别“ CRISPR指导基因编辑的多种结果”,这一过程通常需要长达两个月的昂贵而复杂的DNA分析。
Kmiec告诫说,他们的工作揭示的意外变化涉及到靶向修复的基因组直接位点周围DNA的“细微突变”。他说,这与引起广泛关注的关于CRISPR通过从预期位点向远处漂移并在基因组中随机切割而引起“脱靶”突变的风险的关注截然不同。
主要作者布雷特·桑斯伯里补充说:“重要的是,在所有情况下,我们仍然看到CRISPR达到了甚至在五年前都无法想象的成功修复水平。”“但是我们发现修复位点附近的DNA有许多其他变化,需要更好地理解,以便在纠正一个问题时,我们不会制造另一个问题。”
她说,这些变化包括DNA代码的删除,重复和重新排列。尽管研究人员认为这些意外编辑中的绝大多数可能对患者没有影响,但重要的是要识别它们并确定哪些可能构成风险。例如,Kmiec说,对DNA代码的意外更改(其行为类似于确定基因功能的软件),可以指示基因产生有害的蛋白质。
根据这项研究,“这些信息构成了确定围绕基因工程工具治疗人类疾病有效性的风险收益决策的基础。”
Kmiec说:“ CRISPR可能永远不会是100%完美的。”“但是CRISPR工具正在不断改进。如果我们能够达到70%或80%的精确度-并揭示并理解修复过程中发生的任何变化的重要性,那么我们将更安全地使用CRISPR进行治疗病人。我们希望我们的新工具可以帮助加快实现这一目标的努力。”
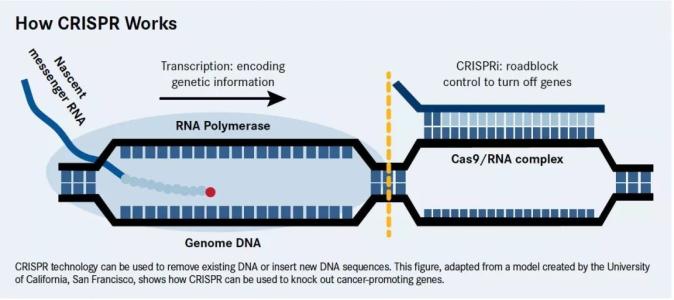
CRISPR代表“成簇的规则间隔的短回文重复序列”。这是一种在细菌中发现的防御机制,可以识别并切碎入侵病毒的DNA。
科学家们已经学会了如何修改这种机制,从而可以直接“编辑” DNA编码的特定序列,重点是修复导致致命疾病的DNA突变。例如,正在进行使用CRISPR修复镰状细胞病患者中产生异常红细胞的基因突变以及导致囊性纤维化患者中粘液破坏性积累的突变的工作。
但是Kmiec指出,大多数用于分析CRISPR基因编辑的工具最适合用于验证修复是否成功,而不是揭示附近DNA链可能发生的改变。他说,要进一步筛选这些意外的编辑内容,需要从细胞中提取和分析大量的DNA编码,这种过程可能需要两个月才能完成。即使这样,它也可能无法捕获所有更改。研究警告说,结果是,当研究人员报告成功使用CRISPR修复有故障的基因时,他们“可能会无意中低估了这项非凡技术的附带活性”。
基因编辑研究所的科学家通过与他们开发的系统一起工作解决了这个问题,该系统可以对从细胞中提取的DNA的环状片段(称为质粒)进行基因编辑。研究人员发现,在质粒或“无细胞”系统中进行的工作消除了细胞内的许多复杂生物活性,这使得很难分离出CRISPR引入的全部DNA变化。
在这项研究中,他们报告说,他们的系统使他们能够“以一种简单明了的方式可视化通过CRISPR指导的基因编辑过程创建的各种各样的遗传修饰”。另外,由于该工具可以快速,经济地筛查编辑结果,因此研究人员指出,该工具使科学家可以执行和筛查多个试验编辑,这比基于细胞的系统的实际操作要多得多。这样一来,他们就可以识别出可能会以相对罕见的频率发生的意外突变,从而避免其他情况的发生。
它还允许他们测试CRISPR的不同变异。当科学家使用CRISPR工具编辑基因时,他们可以使用不同的酶(例如Cas9或Cas12a)进行实际切割,并且通常包括称为模板的DNA“模板”,以用作识别和修复受损代码的图。这项新研究发现,“精确修复”的修复率(无需引入意想不到的突变即可完成修复)根据所使用的酶和模板的不同而有很大差异,范围从5%到64%不等。
开发更好的方法来筛选CRISPR诱导的突变的工作是基因编辑研究所更广泛的努力的一部分,该研究所在编辑从人细胞提取的DNA质粒方面取得了突破性的进展。该团队已经使用他们的“无单元格”方法来同时设计多个编辑。这项工作导致了与一家生物技术公司的合作,以开发个性化癌症护理的新方法。由基因编辑研究所的团队开发的工具可以在人类DNA样本中快速复制单个患者癌症肿瘤的独特而复杂的遗传特征。这些样品可用于筛选多种化学疗法和其他抗癌药物,以设计最适合单个患者的治疗方法。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
6月25-28日,由中国进出境生物安全研究会、中国国际旅行卫生保健协会主办,中国青年创业就业基金会支持,中国出入...浏览全文>>
-
胃肠镜检查,听起来可能有些令人不安,但实际上,它可能是生活中的救命稻草。对于一些人来说,定期进行胃肠镜...浏览全文>>
-
6月16日-20日,2025年优秀博士后研究人员(绍兴)研学活动顺利举行。本次活动汇聚了来自全国各地的百余名博士后,...浏览全文>>
-
近日,天津松果生物医疗科技有限公司自主研发的牛跟腱来源去端肽I型胶原蛋白原材料成功通过国家药品监督管理局...浏览全文>>
-
在数字化产业转型的浪潮奔涌之际,病理学正经历着前所未有的革新机遇。奥伟登(Evident)凭借百年光学技术积淀,以...浏览全文>>
-
6月6-8日,CHINAGUT 2025中国肠道大会在宁波国际会议中心隆重举办。大会由南京医科大学第二附属医院、国家消化...浏览全文>>
-
在第28届北京国际口腔展这一行业风向标级盛会上,北京易岭生物科技有限公司(下面简称易岭生物)凭借重磅新品发...浏览全文>>
-
2025款上汽大众ID 4 X在安徽阜阳地区的售价会根据配置和选装包有所不同。基础版车型的厂商指导价大约在20万...浏览全文>>
-
岚图FREE,作为一款集豪华与智能于一体的新能源SUV,正以全新的姿态迎接每一位渴望高品质出行的用户。现在,岚...浏览全文>>
-
安徽阜阳的大众ARTEON 2022新款现已到店,最低售价从34 80万元起,无疑是近期购车的最佳时机。这款车型以其...浏览全文>>
